TOPLAR DAMAR TIKANIKLIĞI (DVT)
Toplardamar tıkanıklığı pek çok nedene bağlı olarak gelişebilir. En önemli ve ölümcül komplikasyonu pulmoner embolidir. Toplardamar tıkanıklıkları yüzeyel ve derin toplardamar olmak üzere ikiye ayrılırlar.
Pıhtı oluşumu ve yıkımı arasındaki normal denge, anormal pıhtı oluşumuna yol açan belirli genetik veya sonradan kazanılmış kusurların varlığı ile değişebilir.
Genel olarak pıhtı oluşumunda üç faktör söz konusu olup bunlar Virchow triadı olarak adlandırılır.
1. Kan akımında yavaşlama
2. Pıhtılaşmada artış
3. Damar duvarında zedelenme
Bu üç faktörden herhangi birinde olan bir değişiklik anormal pıhtılaşmaya yol açabilir. Derin ven trombozu (DVT) veya pulmoner emboli (PE) için tüm risk faktörleri bu üç kategoriden birine girer. Venöz tromboembolik olay (VTE), aynı hastada bir DVT veya PE veya her ikisinin birlikte olmasıdır.
Yüzeyel toplardamar tıkanıklıkları (Tromboflebit)
Yüzeyel toplardamar tıkanıklığı kendiliğinden, cerrahi veya damardan ilaç tedavilerine bağlı gelişebilir. Gelişme nedeni ve risk faktörleri derin toplardamar tıkanıklığı ile benzerlik göstermektedir. Olguların %10’nunda akciğere emboli (pıhtı atılması) gelişmekte, bunların %20’si ciddi seyretmektedir.
Tedavi
- Olguların önemli kısmında bakteriyel infeksiyon izlenmediği için antibiyotik gerekmeyebilir.
- Antiinflamatuvar tedavi 5-7 gün (ibuprofen)
- Derin ven trombozu gelişebilecek hastalara kan sulandırıcı (antikoagülan tedavi) uygulanır
- Varislerde gelişen pıhtılaşmalarda cerrahi tedavi uygulanabilir
Derin toplardamar trombozları (Tıkanması) (DVT)
- DVT % 90’ı alt ekstremitede olup, en sık uyluk ve dizaltı bölümünde gelişir.
- Klinik olarak % 60’ı sessiz seyreder
- Sol bacakta daha sık gelişmektedir.
- Akciğere pıhtı atılan olguların % 70’inde derin toplardamarda pıhtı saptanır.
- Derin toplardamar tıkanıklığı olan hastaların % 50’den fazlasında akciğerde pıhtı saptanır
 Toplardamar kan akımında yavaşlama nedenleri
Toplardamar kan akımında yavaşlama nedenleri
- Hareketsizlik
- Dört günden daha uzun süreli yatak istirahatı
- Uzun süreli seyahatler
- Omirilik yaralanmasına veya inmeye bağlı felç
- Uzun süreli motosiklet kullanımı
- Bacakta kırık nedeniyle alçıya alınması
- Önceki damar tıkanıklığı
2. Pıhtılaşmaya eğilimde artış
- Kötü huylu tümörler
- İnflamasyon bozuklukları
- Böbrek yetmezliği
- Sepsis
- Estrojen artışı
- Gebelik
- Doğum sonrası < 3 ay
- Düşük yapma, küretaj
- Doğum kontrol ilacı, estrogen kullanımı
- Genetik bozukluklar
Pıhtılaşmaya eğilimi artıran Genetik bozukluklar
Kimlerde genetik risk faktörleri araştırılmalıdır;
- Nedeni bilinmeyen 40-45 yaşından önce spontan gelişen tromboembolik hadiseler
- Alt ekstremite dışında gelişen trombozlar
- Tekrarlayıcı ve gezici veya massif trombozlarda
- Aile öyküsü olanlarda
- Warfarine bağlı cilt nekrozu gelişenlerde
Doktorlar artık kalıtsal bir pıhtılaşma bozukluğu tetkik etmek için çeşitli testlere sahiptir. Hangi hastalara hangi testlerin yapılması gerektiği ve pozitif sonuçların ne anlama geldiği konusunda tartışmalar vardır. Bu bölüm en yaygın pıhtılaşma bozukluklarını gözden geçirmektedir.
Pıhtılaşma Bozuklukları
İki tip pıhtılaşma bozukluğu vardır. Birincisi kalıtsal bir hastalıktır, bir veya iki ebeveynden geçmiştir. İkincisi kazanılmış bir hastalıktır; hasta doğduğunda mevcut değildir, fakat daha sonraki yaşamında gelişir.
Kalıtsal Pıhtılaşma Bozuklukları
Kalıtsal pıhtılaşma bozuklukları 2 grupta ortaya çıkar:
Grup 1: Kanda pıhtılaşma önleyici faktörlerin eksikliği
Grup 2: Kanda yüksek miktarda pıhtılaşma faktörünün olması
Grup 1 pıhtılaşma bozuklukları anti-trombin eksikliği, protein C eksikliği ve protein S eksikliğini içerir. Grup 2 pıhtılaşma bozuklukları, aktive protein C direncini (Faktör V Leiden mutasyonu), protrombin G20210A mutasyonu ve yüksek seviyelerde Faktör VIII, IX ve XI ‘u içerir. Genel olarak, Grup 1 bozuklukları daha az yaygındır, fakat grup 2 bozukluklarından daha fazla anormal pıhtılaşmaya neden olur. Grup 1 bozukluğu olan hastalar genellikle ilk DVT'lerini genç yaşta geçirir, tekrarlama olasılığı daha yüksektir ve ailesinde DVT veya PE öyküsü olması grup 2'ye göre daha yüksektir.
GRUP 1 HASTALIKLARI
KANDA PIHTILAŞMA ÖNLEYİCİ FAKTÖRLERİN EKSİKLİĞİ
Antitrombin Eksikliği
Antitombin III eksikliği (AT III): Karaciğerde sentezlenir, etkisini koagülasyon faktörlerinden faktör II, Xa, IXa ve XIIa yı inhibe ederek gösterirler. Heparin tarafından aktivasyonları bin kat artış göstermektedir. Pek çok edinsel hastalığa bağlı olarak da AT III düşüklüğü gelişebilmektedir. Bunlar; heparin kullananlarda, nefrotik sendromda, doğum kontrol hapı kullananlarda ve postoperative dönemde düşüklük görülebilir. Hastalık otozomal dominant geçen 100 den fazla mutasyonu bildirilmiştir. AT III eksikliği kalıtsal trombofilik hastalıkların en trombojenik olanıdır. Bu bozukluğu olan çoğu hasta 30 yaşına kadar bir DVT geçirecektir. Hastaların %80’ninden fazlası 50 yaşından önce tromboembolik hadise yaşarlar. Antitrombin eksikliği, genel popülasyonun % 0.07-0.2'sinde ve DVT’si olanların % 0.5-8'inde bulunur.
Kandaki antitrombin miktarı test edilebilir. Testler VTE'nin başlamasından 3 ay sonra ve kan sulandırıcı ilaç kesildikten en az 5 gün sonra yapılmalıdır. Bunun nedeni kan sulandırıcıların kandaki antitrombin seviyelerini etkilemesidir. Diğer birçok durum da antitrombini etkileyebilir.Bu nedenle test sonuçları hastadan alınan tıbbi öykü ile yorumlanarak değerlendirilmelidir.
Antitrombin eksikliği DVT için güçlü bir risk faktörüdür. DVT geçirme riski, antitrombin eksikliği olan çoğu insanda 5 ila 50 kat artmıştır. Bu eksiklikle ilgili arterlerde anormal pıhtılaşma olduğu bildirilmiştir. Ancak bu durumu olan kişiler nadirdir ve antitrombin eksikliği ile ilişkisi anlaşılır değildir.
Antitrombin eksikliği olan hastalar heparin tedavisine dirençlidir, çünkü heparinin çalışması için antitrombin varlığı gerekir.Heparin yaygın olarak intravenöz kullanılan bir kan sulandırıcıdır. Kan sulandırıcı kullanması gereken antitrombin eksikliği olan hastalara antitrombin varlığına gerek duymayan başka bir kan sulandırıcı türü verilmelidir. Gerekirse antitrombinin kendisi de verilebilir. Bir VTE meydana geldikten sonra,genellikle ömür boyu oral antikoagülasyon tavsiye edilir.
Protein C Eksikliği
Protein C (PC): protein C K vitaminine bağlı bir glikoprotein olup, karaciğerde sentezlenmektedir. Temel etki mekanizmasını faktör Va ve VIIIa’yı inhibe ederek gösterirler. Pıhtılaşma işlemi esnasında, C proteini aktive edilir ve S proteini ile birlikte pıhtılaşma işlemini kontrol altında tutmak için kan sulandırıcı olarak işlev görür. Protein C'deki eksiklik, pıhtılaşma sürecini kontrol altında tutma yeteneğinde azalmaya neden olur ve anormal pıhtı oluşumu ile sonuçlanır.
Protein C eksikliği, popülasyonun% 0.4'ünde ve DVT veya PE'li hastaların yaklaşık% 4'ünde mevcuttur.
Kandaki C proteini miktarı bir kan testi ile ölçülür. Test varfarin tedavisi durdurulduktan 2-4 hafta sonra yapılmalıdır. Birçok neden C proteininin düşük olmasına yol açabilir. Örneğin; yeni pıhtı oluşumu, düşük K vitamini, karaciğer hastalığı, şiddetli enfeksiyonlar (sepsis), böbrek yetmezliği, ameliyat sonrası durum, kemoterapi sonrası meme kanseri hastaları,masif kanamalar.
Normal testlerde PC aktivitesi %70-140 arasında değişmektedir. Heterozigot olanlarda PC aktivitesi %50’den, homozigotlarda ise %5’den az olarak izlenmektedir.
Hastalarda normal bir protein C seviyesi hastalığı dışlar, ancak protein C seviyesinin düşük olduğu durumda tedavi tamamlandıktan sonra seviyesinin tekrar kontrol edilmesi gerekir. Protein C eksikliği olan kişilerin DVT veya PE yaşama olasılığı genel popülasyondan yaklaşık 3 kat daha fazladır. Protein C eksikliğine sahip olanların yaklaşık % 50'si 40 yaşına kadar, bir DVT veya PE atağı geçirecektir. Bu hastalarda artardamar da pıhtı oluşumu ile ilgili önemli derecede artmış bir risk yoktur.
Eğer bir insan protein C eksikliğine sahipse ve hiç bir zaman VTE geçirmemişse ilaç kullanması gerekli değildir. Ameliyat ve VTE riskinin yüksek olduğu durumlarda VTE'yi önlemek için kan sulandırıcı kullanmaları gerekir. Protein C eksikliği olan bir kişinin VTE'si varsa, kan sulandırıcı alması gerekir.
Protein C eksikliği olan hastaların varfarin (oral kan sulandırıcı) başlamadan önce heparin gibi hızlı etkili kan sulandırıcı kullanması önemlidir. Başlangıçta tek başına varfarin kullanımında, hastaların azında uygun seviyelere ulaşıldı. Bu nedenle varfarin seviyesi yeterli olana kadar başlangıçta hızlı etkili bir antikoagülan kullanılır ve sonrasında kesilir.
Protein S Eksikliği
Protein S vücudun doğal pıhtılaşma sürecini kontrol altında tutmak için protein C ile etki eder. Düşük protein S seviyesi düşük protein C seviyesi ile benzer etkilere sahiptir.
Esas olarak protein C’nin fak Va ve VIIIa’yı inhibisyonunda kofaktör olarak rol alır.Genel popülasyonun yaklaşık % 0.2'si protein S eksikliğine sahiptir. DVT'li veya PE ‘si olan kişilerin % 5'i protein S eksikliğine sahiptir.Testlerde protein S aktivasyonu %70-140 arasındadır.Aktivasyonun %30’un altında olması kalıtsal eksikliği düşündürür.
Protein S seviyesi bir kan örneğinden test edilebilir. Ancak, bunun teşhisi zor olabilir, çünkü pek çok şey protein S seviyesini etkileyebilir. Azalmış protein S ile bağlantılı durumlar; varfarin ve oral kontraseptif kullanımı, gebelik, karaciğer hastalığı, nefrotik sendrom ve şiddetli pıhtı oluşumudur. Yeni bir pıhtı oluşumu sırasında testin normal olması hastalığı dışlar, ancak test anormal sonuçlanırsa varfarin tedavisi kesildikten 2-4 hafta sonra tekrarlanmalıdır. Düşük molekül ağırlıklı heparin kullananlarda ise son dozdan 12-24 saat sonra bakılmalıdır.
Protein S eksikliği ile birlikte DVT veya PE’de değişken oranlar bildirilmiştir.Çok nadir olduğu için çalışmak zordur. Protein S eksikliğinde VTE geçirme riski 10 kat arttığı bildirilmiştir. Protein S eksikliğinin arteriyel pıhtı oluşumunu artırdığına ait kanıt yoktur.
Protein C eksikliğinde olduğu gibi, hiç VTE geçirmemiş protein S eksikliği olan hastalar herhangi bir spesifik tedaviye ihtiyaç duymaz, ancak VTE geçirme riski olabilecek bir durum varsa koruyucu kan sulandırıcı kullanmaları gerekir.
VTE atağı olan bir kişinin, varfarin gibi daha uzun süreli kan sulandırıcılarına başlamadan önce heparin gibi hızlı etkili bir kan sulandırıcı kullanması gerekir.
Grup 2 HASTALIKLARI:
KANDA PIHTILAŞMA ÖNCÜSÜ FAKTÖRLERİNİN ARTMIŞ MİKTARI
Aktif Protein C Direnci / Faktörü V Leiden Mutasyonu
Fak V karaciğerde sentezlenir. Aktive olmuş protein C, Fak V’i proteolize uğratarak antikoagülan etki gösterir. Aktif Protein C direnci, Faktör V'in, pıhtılaşma reaksiyonundaki direncini belirtir. Aktifleştirilmiş C proteini pıhtılaşma reaksiyonu yavaşlatmak için Faktör V üzerinde etkili olmazsa pıhtılaşma riskinde artışa neden olur. APC direncinin çoğu, buradaki bir mutasyon olan Faktör V Leiden mutasyonundan kaynaklanmaktadır ve bu Faktör V ‘i kodlayan gendeki mutasyondur.
Faktör V Leiden en sık görülen genetik kan pıhtılaşma bozukluğudur.Özellikle Kafkas veya Avrupa kökenli insanlarda yüksek oranda görülme olasılığı mevcuttur. Kafkasyalıların yaklaşık % 5'i, Afrikalı Amerikalıların % 1,2'si, İspanyol Amerikalıların % 2,2'si, Yerli Amerikalıların % 1,2'si ve Asyalı Amerikalıların % 0,45'inde görülür. VTE'li hastaların % 10-20’si bu gen mutasyonuna sahiptir.
Faktör V'in APC'ye dirençli olup olmadığını gösteren bir test ve Faktör V Leiden mutasyonu için genetik bir test mevcuttur. Her iki test de durumu teşhis edebilir.
APC direnci, anormal pıhtı oluşumu için nispeten zayıf bir risk faktörüdür. Faktör V için bir anormal gen (heterozigot) 8 kat artmış pıhtılaşma riskine sahiptir ve her iki gende anormal ise (homozigot) riskte 80 kat artış vardır. Faktör V için bir anormal geni olan hastalarda yaşam boyu semptomatik DVT veya PE geçirme olasılığı yaklaşık % 10'dur.
Bununla birlikte, APC direncine sahip bir kişi için anormal pıhtı oluşumunu artıran oral kontraseptif kullanımı, hormon replasman tedavisi veya gebelik gibi başka risk faktörleri de vardır. APC direnci tekrarlayan gebelik kaybı ve obstetrik komplikasyon riskini artırabilir. Ayrıca, böbrek nakil alıcıları ile ilgili de kötü sonuçlarla ilişkilidir. Bu durumun arterlerdeki anormal pıhtı ile ilişkili olup olmadığı bilinmiyor.
Protrombin gen mutasyonu (G20210A)
Protrombin G20210A mutasyonu,protrombin genindeki kalıtsal bir kusurdur. Protrombin, kandaki pıhtı oluşumuna yardımcı olan bir proteindir. Yüksek düzeyde protrombin seviyesine sahip kişide anormal pıhtı oluşma riskini artmıştır.
Bu hastalık ikinci en yaygın görülen kalıtsal pıhtılaşma bozukluğudur. Kafkasyalıların % 2'si, Güney Avrupa kökenli insanların % 3'ünde görülür ve Yerli Amerikalılar, Asyalı Amerikalılar veya Afrika kökenli Amerikalılar’da nadir olarak görülür.VTE geçiren hastaların % 5 ila 10'unda görülür.
Gendeki bozukluğu bulabilen bir kan testi vardır. Bu test bir pıhtı oluşmadan önce, pıhtı oluşma süresince veya sonrasında herhangi bir zamanda doğru olarak gerçekleştirilir. Heterozigot taşıyıcılarda 1,5, homozigot taşıyıcılarda ise 2 misli pıhtılaşmaya eğilim artmaktadır. Gebelikte ise venöz tromboembolizm riskini 15 kat artış görülmektedir.
Bu protrombin gen mutasyonuna sahip çoğu hasta, 50 yaşına kadar VTE atağı geçirmez. Bu bozukluğu olan hastalarda pıhtılaşmanın yarısı şu durumlarda görülür: cerrahi, travma, uzun süreli immobilizasyon, gebelik veya östrojen tedavisi.Bu bozukluğun atardamarda anormal pıhtılaşma riskini arttırdığı görülmemektedir.
Hiperhomosisteinemi
Hiperhomosisteinemi, homosistein amino asidinin kazanılmış veya kalıtsal bir yükselmesini ifade eder. Amino asitler, vücuttaki proteinlerin yapı taşlarıdır. Homosistein, çeşitli amino asit türlerinden biridir. Kazanılmış hiperhomosisteinemi böbrek yetmezliği, hipotiroidizm, folat eksikliği, B6 Vitamini veya B12 eksikliği gibi bazı tıbbi durumlarla ortaya çıkabilir.
Kalıtsal hiperhomosisteinemi, homosisteini parçalayan enzimleri kodlayan genlerdeki mutasyonlardan kaynaklanır. Azalan metilentetrahidrofolatredüktaz (METHFR) üretim ve aktivitesine bağlı olarak homosistein yükselir. Buna bağlı tromboz riski artış gösterir. Hiperhomosisteinemi hem arter hem de vende pıhtılaşma problemleriyle ilişkilidir. Hiperhomosisteineminin kan pıhtılaşmasını nasıl etkilediği tam olarak bilinmemektedir.
Genel popülasyonun % 50'sine kadar olan kısmı, homosistein metabolizmasını etkileyen bir mutasyona sahip olabilir. Bu her durumda yüksek homosistein seviyelerine neden olmaz.
MTHFR gen mutasyonu: çok sayıda mutasyonu bulunmakta olup en sık görüleni C677T ve A1298C dir.
Hiperhomosisteinemi tanısı homosisteinin kan düzeyine dayanır. Yeni bir VTE olayından birkaç ay sonra homosistein düzeyi yükselebilir. Testlerin doğru olması için VTE saptandıktan bir kaç ay sonra yapılmalıdır.
Hiperhomosisteinemi hem arter hem de vende anormal pıhtılaşma ile ilişkilidir. Hiperhomosisteinemi'nin sadece pıhtılaşma belirtisi ya da pıhtılaşma nedeni olup olmadığı açık olmasa da pıhtılaşmada etkisi vardır. Homosistein seviyesi ilaçla azaltılabilir, ancak bu VTE riskini değiştirmez, bu nedenle bu durum için testin değeri belirsizdir.
Folik asit, B6 vitamini ve B12 vitamini tedavisi ile yüksek homosistein düzeyleri azaltılabilir.
Diğer Kalıtsal Pıhtılaşma Bozuklukları
Henüz tam olarak bilinmeyen başka kalıtsal pıhtılaşma bozuklukları vardır. Bu rahatsızlıkların çoğu DVT ve PE tanısı almış kişilerde VTE riskini artıran ‘bilinmeyen’olarak adlandırılan rahatsızlıklar olduğu düşünülmektedir.
Antifosfolipid Antikor Sendromu (APS)
Antifosfolipid antikorları, kandaki pıhtılaşmada önemli olan proteinlere karşı yönlendirilen bir antikorlar ailesidir. Bu antikorlar lupus antikoagülanları ve antikardiolipin antikorları içerir. Primer APS hastaları APS'ye sahiptir ancak bu hastalarda lupus veya diğer otoimmün hastalıkları bulunmaz. Sekonder APS, APS ve sistemik lupus eritematozus (SLE) hastalarını içerir.
Bu durum sağlıklı bireylerin sadece % 2'sinde bildirilir, ancak VTE’ li hastaların % 20'sinde görülür.
Bu durumun teşhisi hem klinik hem de laboratuvar testlerine dayanır.Bu duruma tanı koyabilmek için bir kişide,en az 6 hafta arayla bakılan iki testte antikor düzeylerinde yükselme olmalıdır. Anormal pıhtılaşma veya gebeliğe bağlı bir komplikasyona sahip olmalıdır.
APS'li kişilerde VTE riski nispeten yüksektir. APS li kişilerin yaklaşık 1/3'ünde anormal pıhtılaşma olayı olmuştur. Genellikle bu olay bir DVT'dir. Lupusu olmayan APS'lerde, VTE riskinde APS olmayanlara göre 11 kat artış var. Ayrıca arteriel pıhtı oluşumu riski de artmıştır. Lupusu olan hastalarda antikorlar olmasa bile anormal pıhtı oluşumu riski artar.
İlk VTE'si olan APS hastaları genellikle kısa süreli etkili heparin gibi kan sulandırıcı ile tedavi edilir. 5 gün sonra varfarin tedavisine geçilir. İlk pıhtılaşma olayından sonra kan sulandırıcının ne kadar süre devam edilmesi tartışmalı bir konudur. Bu süre 12 ay ile ömür boyu arasında değişebilir. VTE’si olmayan APS'li hastalarda günlük aspirin tedavisi önerilir, ancak ek risk faktörleri varsa varfarin veya heparin tedavisi düşünülmelidir.
Heparin kaynaklı trombositopeni
Heparin kaynaklı trombositopeni (HIT), heparin tedavisinin ciddi bir yan etkisidir ve bu anormal pıhtılaşmaya neden olabilir. Bu durum, insanın vücudunda heparine karşı antikor oluşturur ve bu antikor aynı zamanda trombositleri de hedefler. Antikor trombositlere bağlanarak kümelenmelerine neden olur, bu da pıhtı oluşturur.
Her ne kadar heparine bağlı antikorlar heparin alan kişilerin % 10-20'sinde ortaya çıksa da, bu hastaların çoğunda HIT gelişmez. 5 gün boyunca heparin kullananların sadece % 1-3'ünde HIT ortaya çıkar. 14 günlük sürekli kullanımın ardından bu oran % 6'ya kadar çıkabilir. Düşük moleküler ağırlıklı heparin kullanımı daha düşük HIT riskine sahiptir.
Heparin tedavisi altındaki bir kişide yeni bir pıhtı oluşması HIT için şüphelidir. Kandaki trombosit sayısında düşme, HIT'in bir başka işaretidir. Heparin tedavisinin başlamasından 5 ile 10 gün sonra trombosit sayısı düşmeye başlar, 7-14 gün sonra düşük bir seviyeye ulaşır. Bu "tipik başlangıçlı HIT’’ olarak bilinir. ‘’Gecikmeli başlangıçlı’’ HIT’de trombosit sayısı heparin tedavisi başladıktan 20 gün sonra düşmeye başlar ve heparin tedavisi kesildikten sonra da düşmeye devam edebilir. “Hızlı başlangıçlı’’ HIT’de, heparine başladıktan sonraki 24 saat içinde trombosit sayısında düşme ortaya çıkabilir. HIT daha önce heparin tedavisi alan hastalarda ortaya çıkabilir. Trombosit sayısında %50 lik düşüş veya trombosit sayısının 100.000'in altına düşmesi HIT için şüpheli olarak kabul edilir. HIT tanısı koymak için gerekli laboratuvar testleri yapılması gerekiyor. HIT için bazı testler vardır ve trombosit fonksiyonu ve otoantikorlara bakılıyor. Eğer bir hasta HIT den şüpheleniliyorsa, test sırasında heparin tedavisinin derhal durdurulması gerekir.
HIT hastalarında anormal pıhtı oluşumu 30 kat artmıştır.En yaygın görülen pıhtılaşma olayı DVT'dir. PE bu hastalarda da yaygındır. Anormal arter pıhtılaşması daha az görülmektedir. HIT'li hastalarda yaklaşık % 20 oranında anormal cilt lezyonları oluşabilir.
Yapılacak ilk şey, tüm heparin kaynaklarını durdurmaktır. Ayrıca anormal pıhtı oluşumunu önlemek için başka bir kan sulandırıcı kullanmak gerekir. Başka kan sulandırıcı olarak lepirudin, argatroban ve bivalirudin kullanılabilir. Düşük moleküler ağırlık heparin bir heparin türevidir ve kullanılmamalıdır. Trombosit sayısı normal değere ulaştığında, varfarin tedavisi başlatılabilir, ancak 5 gün boyunca diğer kan sulandırıcı ile birlikte kullanılmalıdır. HIT olan bir kişi, çok özel ve nadir bir durum olmadıkça yaşamlarında tekrar heparin tedavisi almamalıdır.
Venöz tromboemboli riskini artırabilecek birçok farklı faktör vardır. Bu faktörlerden bazıları riski diğerlerinden daha fazla arttırır. Bu risk faktörleri nedeni bilinmeyen venöz tromboembolik hadiselerde araştırılmalıdır.
3. Damar duvarında zedelenme
- İntravenöz ilaç bağımlılığı
- Travma
- Santral beslenme
- Yatak istirahati
Diğer nedenler
- Yeni geçirilmiş cerrahi
- Yaşın 60’ın üzerinde olması
- Kalp hastalığı
- Obezite
- Bacakta ciddi atardamar hastalığı olması
Klinik bulguları
Ani ağrı ve hareket kısıtlığı başlar. Bacakta ileri ödeme bağlı nadir olarak, gangren, şok ve ölümle sonuçlanabilen tablo gelişebilir.Bacaktaki pıhtı akciğere atılmasına bağlı yan ağrısı, solunum sıkıntısı ve kanlı öksürük gelişebilir.
Geç dönemde, toplardamar içerisindeki kapakçıkların harabiyetine bağlı ödem ve ülseri gelişir.

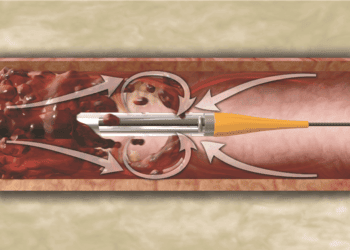
Resim 1. Derin toplardamar tıkanıklığı
Toplardamar tıkanıklığı şühesi veya saptanan hastalara sorular;
- Daha önce sizde veya ailenizde bacakta veya akciğerde pıhtı gelişimi oldu mu?
- Yakın zamanda uzun süreli seyehat yaptınız mı?
- Üç günden daha uzun süreli yatak istirahati yaptınız mı?
- Son 2-3 ay içerisinde cerrahi veya travma geçirdiniz mi?
- Son 3 ay içerisinde gebelik mevcut mu? (Düşük, küretaj)
- Doğum kontrol hapı kullanıyormusunuz?
- Sigara kullanıyormusunuz.
- Başka herhangi bir sağlık probleminiz varmı (kanser, romatizmal, kalp yetmezliği)
- Göğüs ağrısı ve nefes darlığınız var mı?
Derin ven trombozunun tanısı
Toplardamar tıkanıklığı düşünülen hastalarda kesin tanı Doppler ultrason yapılarak oldukça kolay olarak konulmaktadır.
D Dimer Seviyesi Nedir?
D-dimer, pıhtı yıkımının bir ürünüdür. D-dimer seviyesi DVT ve PE geçirmek için gerçek bir risk faktörü değildir, ancak bir DVT veya PE bulunduğunda değeri yükselebilir. D-dimer seviyesi, düşük DVT şüphesi olduğu zaman DVT'yi “ekarte etmek” (mevcut olmadığını göstermek) için kullanılır. Bunun nedeni, seviyenin normal olması durumunda DVT'nin olması muhtemel değildir. Bununla birlikte, seviye yüksekse, DVT mevcut olabilir veya olmayabilir. Yüksek D-dimer seviyeleri anormal pıhtı varlığını gösterebilir, fakat kan seviyesi geçirilmiş ameliyat, kanama, travma, hamilelik, kanser veya arterdeki anormal kan pıhtısı gibi diğer nedenlerle de yükselebilir.
Derin ven trombozu’nun tedavisi
- Bacağın yükseltilmesi (Kalp seviyesi üzerinde tutulur.)
- Kan sulandırıcı ve pıhtı önleyici tedavi (Antikoagulasyon) : İlk 1 hafta damardan pıhtı önleyici tedavi (heparin), takiben 3 ay tablet (oral antikoagulan) kullanılır
- 3-4 gün sonra mobilizasyon
- Pıhtı eritici tedavi:Derin toplardamardaki trombozun (pıhtının) erken ve hızlı ortadan kaldırılması için ilk tercih, kateter yönelimli trombolizdir (pıhtı eritici). Bu tedavinin iki temel unsuru bulunmaktadır. Birincisi; pıhtının mekanik olarak parçalanması ve ikincisi de pıhtının kimyasal olarak eritilmesidir. Mekanik yöntemler ile parçalanma pıhtı içerisine pıhtı eritici ilaçların nüfuz etmesini kolaylaştırır. İlk üç gün içinde %45 oranında başarı sağlanır.
- Varis çorabı giydirilir.
Derin toplardamar tıkanıklıklarında damar açma yöntemleri
Bacakta oksijenini kaybetmiş kirli kanı taşıyan yüzeyel ve derin olmak üzere iki toplardamar (ven) bulunmaktadır. Derin toplardamarımız bacaktan gelen kirli kanın %90’nını taşımaktadır. Akut derin venöz trombozu (DVT), bir veya daha fazla toplardamarda pıhtısı oluşumudur.
Derin toplardamar tıkanıklığının %60’ı baldır gölgesinde, %40’ı ise kasık ve karın içi bölgede izlenir.
Yaygın derin ven trombozu, akut ağrıya, şişmeye ve bacaklarda renk değişikliğine neden olur. Bu tablo da akut dönemde;
- Bacakta kasıktan itibaren ciddi ödem, ağrı, kızarıklık gelişir
- İleri ödeme bağlı bacağın beslenmesi bozulur ve gangren gelişebilir
- Akciğer embolisine yol açabilir
- İlk 15 gün içerisinde pıhtı çeşitli derecelerde ortadan kalkabilir, akım başlayabilir, bacak rahatlayabilir.
Kronik dönemde;
- Pıhtıya bağlı tıkanıklık kronik olarak devam edebilir
- Pıhtının uzun süre içerisinde çeşitli derecelerde açılmasına rağmen kapakçıkların bozulması ve buna bağlı derin venöz yetmezlik gelişir.
Kronik dönemde tıkalı veya açık ciddi venöz yetmezliği bulunan hastalarda posttrombotik sendrom denilen tablo açığa çıkar. Bu tablo akut dönemde gördüğümüz problemler kronik olarak artarak devam eder. Bu tabloda bacak toplardamarlarındaki yüksek venöz basıncın etkisine bağlı; ileri ödem, özellikle bilek bölgesinde renkte koyulaşma, sertleşme ve ülserler gelişir. Bu tablo önlem alınmadıkça daha problemli hale gelir.
Bundan dolayı özellikle kasık ve yukarısında ortaya çıkan derin ven trombozlarında hastayı akut ve kronik dönemde ortaya çıkan problemlerden korumak için erkenden damarı açmaya yönelik girişimler çok faydalı olacaktır.
Sistemik pıhtı eritici ilaç kullanımı (Tromboliz)
Normalde damar içerisinde oluşan pıhtılar, aynı zamanda pıhtı eritici sistemi aktive ederler ve buna bağlı pıhtı parsiyel veya tamamen eriyebilir. Bu süreci hızlandırmak ve tama yakın açılma sağlamak amacıyla pıhtı eritici sistemi uyaran plazminojen aktivatörü olarak bilinen ilaçlar kullanılır. Bu ilaçlar pıhtı içine hapsolmuş plazminojeni aktive ederek plazmin denilen aktif formuna çevirirler. Plazmin ise organize olmuş pıhtı olan fibrin'i parçalayarak etki eder. Parçalanmış fibrin ürünleri vücuttan dolaşım yoluyla uzaklaştırılır.
Damardan sistemik dolaşıma verilen plazminojen aktivatörü, vücudun tüm bölgelerine eşit miktarda (sistemik tromboliz) dağılır. Ancak bu uygulamaya bağlı verilen ilaç pıhtı içerisine yeterli dozda nüfuz edemez ve vücudun diğer bölgelerinde kanamaya yol açabilir. Bundan dolayı, bu ilaçlar hem etkinliği artırmak, hem de kanama riskini azalmaya yönelik olarak bir katater yardımıyla direk pıhtı içine verilebilir. Bu yöntemin de daha az olmakla birlikte vücudun herhangi bir yerinde kanamaya yol açabilir. Özellikle geçirilmiş ameliyatı bulunan hastalarda kanama riski artış gösterir.
Katater aracılığı ile direk pıhtı eritici ajan uygulanması
Son zamanlarda yayınlanan çalışmalara göre, iliofemoral derin ven trombozu tedavisinde geleneksel antikoagülasyon ile başarı %18 iken bu oran kateter-yönlendirmeli trombolizle ile %80 lere çıkabilmektedir. Özellikle iliofemoral DVTsi olan hastalarda zamanında başarılı damar açmaya yönelik işlemlerin ileride gelişecek olan posttrombotik sendrom’u engelleyerek yaşam kalitesini ciddi şekilde düzelttiği gösterilmiştir.
Perkütan mekanik trombektomide, pıhtıyı mekanik olarak parçalayarak plazminin pıhtıya daha fazla nüfuz etmesi sağlanabilmektedir. Bir cihazlar, küçük parçalara ayrılmış pıhtıyı vücuttan uzaklaştırırlar.
Eğer tromboliz'e bağlı riski çok yüksekse, cerrahi olarak direk venöz trombektomi önerilir.
Yatalak olan ve çok sağlıksız olan hastalar için, tek başına antikoagülasyon ajanları (kan inceltici ajanlar) ile tedavi önerilebilir.
Sol ana atardamarın sol ana toplardamara basısına bağlı sol bacakta gelişen trombozlarda pıhtının temizlenmesini takiben yeniden oluşmaması için bası bölgesine stent yerleştirilmesi uygun olacaktır.
İşlemi takiben pıhtı önleyici ilaçları damardan birkaç gün verilir ve takiben uzun süreli kullanılmak üzere ağızdan verilirler
Katater aracılığı ile direk pıhtı eritici ajan uygulanması
Derin toplardamar tıkanıklığı ile gelen hastada pıhtı eritici kullanılmasında herhangi bir sakınca yoksa, bacaktan diz altı bölgeye derin toplardamara lokal anestezi ile ultrason eşliğinde katater yerleştirilerek buradan yaklaşık 24-48 saat boyunca veya daha uzun süreler pıhtı eritici madde uygulanır. Bu uygulama ile önemli ölçüde hastada damar tamama yakın açılabilmektedir.
EKOS: Ekosonik sistem
Düşük enerjili, yüksek frekanslı ultrasonik ses dalgaları kullanılarak pıhtı eritici ajanların pıhtıya olan geçirgenliği artırılması sağlanır. Lokal anestezi eşliğinde dizaltı bölgeden yerleştirilen katater içerisinden kılavuz tel gönderilir. Bu kılavuz tel üzerinden ultrasonik katater ilerletilerek pıhtının başlangıcına kadar ilerletilerek ultrasonik ses dalgaları ile birlikte pıhtı eritici uygulanır. Yaklaşık 24-48 saat uygulanır. Bu yöntem ile başarı oranı direk uygulamaya göre biraz daha yüksektir. Ayrıca bu yöntemde pıhtı mekanik olarak parçalanmadığı için emboli riski düşük olup kapakçıklara zarar vermez.
Anjiojet farmakomekanik sistem
Pıhtıyı parçalayarak ortamdan vakumlayan cihaz. Yüksek hızla çalışan cihazdan serum fizyolojik sıvısı pıhtı duvarına çarparak parçalanması sağlanırken, aynı zamanda aspire edilir.
Birlikte çok düşük miktarda pıhtı eritici verilerek pıhtının daha kolay çözülmesi sağlanır. Lokal anestezi altında bacak arkasından diz altı bölgeden lokal anestezi ile katater yerleştirilerek burdan gönderilen anjiojet ile yaklaşık 10-20 dakikada damar içerisindeki pıhtı temizlenir.
Akut toplardamar trombozun temizlenmesi esnasında gelişen komplikasyonlar
Siştemik tromboliz işlemi uygulanırken en büyük komplikasyonu kanamadır. En sık kataterin toplardamara giriş yerinden veya işlem esnasında damarın yaralandığı bölgelerden kanayabilir. En korkulan kanama şekli ise inmeye yol açan intrakranial (beynin içinde) kanamadır. İşlem esnasında pıhtı parçalara bölündüğü için nadir olarak pulmoner emboli gelişebilir. Bu risklere, mekanik trombektomi cihazları kullanıldığında da dikkat edilmelidir.
Cerrahi trombektomi
Cerrahi genellikle sadece çok semptomatik olanlarda veya diğer yöntemler başarısız olduktan sonra kullanılır, bu nedenle beklenen sonuçlar etkileyici olmayabilir. Posttrombetik sendrom, ataktan 10 yıl sonraki incelemede, ameliyat olan hastaların yaklaşık % 30'unda, sadece kan sulandırıcı kullanılan grubun ise % 70'inde geliştiği saptandı.
Prof.Dr.ilhan Gölbaşı

 Toplardamar kan akımında yavaşlama nedenleri
Toplardamar kan akımında yavaşlama nedenleri